近日,基础医学院人体解剖学系靳建亮教授课题组在《先进科学》(Advanced Science)在线发表了题为《Bmi-1 通过表观遗传机制调控骨髓间充质干细胞的成骨和成脂分化以延缓骨衰老》(Bmi-1 Epigenetically Orchestrates Osteogenic and Adipogenic Differentiation of Bone Marrow Mesenchymal Stem Cells to Delay Bone Aging)的研究论文,首次发现Bmi-1在骨髓间充质干细胞(BMSCs)分化的表观遗传调控中发挥着枢纽蛋白作用,通过促进BMSCs的成骨分化并抑制其成脂分化来延缓骨衰老。该研究将为由Prx1驱动的BMSCs中Bmi-1过表达防治老年性骨质疏松症(SOP)提供临床转化依据。

SOP是一种系统性、进行性疾病,其特征包括细胞衰老、骨密度降低、骨微结构退化,骨脆性和骨折风险增加。与绝经后骨质疏松症不同,SOP 主要是由细胞衰老所引起,因此对老年男性和女性的健康均有显著影响。随着全球人口老龄化持续加深加快,SOP已成为重要的公共卫生问题。因此,需要深入研究SOP的发病机制,以找到新的治疗靶点。尽管一些研究报道了表观遗传修饰在BMSCs分化过程中的作用,但仍需进一步探索表观遗传调控BMSCs向成骨和成脂分化以延缓骨衰老的关键核心分子。
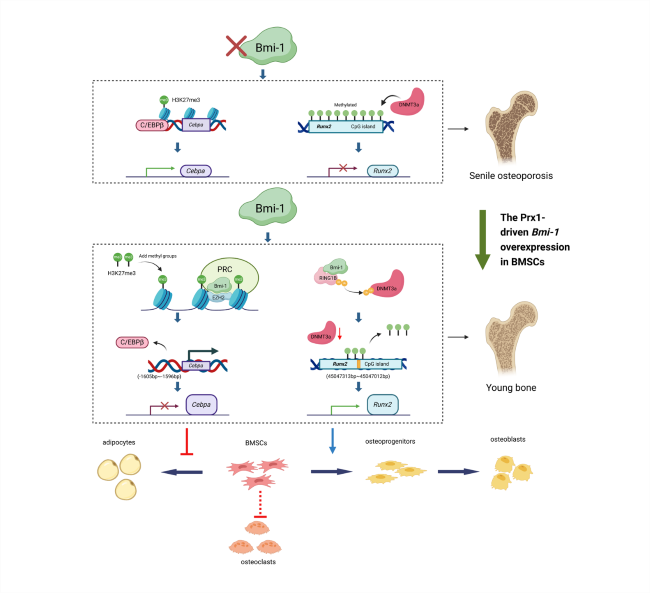
本研究通过对于衰老与年轻的人源BMSCs的RNA测序数据进行分析,富集到了衰老导致BMSCs分化的关键表观分子信号多梳抑制复合物(PRC)2的组蛋白甲基化效应。作为PRC1中的主要成员,Bmi-1在调节细胞周期和预防细胞衰老方面起着至关重要的作用。作者先前发现Bmi-1全基因敲除小鼠出现了成熟前衰老的SOP表型,表现出骨生长迟缓、骨形成减少和脂肪细胞形成增加。并进一步观察到Bmi-1在BMSCs衰老和成脂分化中表达下调,而在成骨分化过程中表达上调。所以,作者聚焦到了Bmi-1对于BMSCs分化的表观遗传调控。为了观察Bmi-1阳性的BMSCs在长骨中的定位,作者构建了多种转基因动物模型,并发现 Prx1驱动的BMSCs中Bmi-1敲除虽不影响骨长度,但它通过抑制成骨细胞骨形成、促进破骨细胞骨吸收、下调BMSCs的增殖及其向成骨分化,并上调BMSCs的成脂分化来减少骨量并增加骨髓脂肪,导致SOP表型。进一步研究发现,Bmi-1-RING1B通过与DNA甲基转移酶DNMT3A结合,促进其泛素化降解,进而抑制调控成骨分化的转录因子Runx2的DNA甲基化,从而上调Runx2表达以促进BMSCs向成骨细胞分化。同时,Bmi-1-EZH2通过促进成脂分化转录因子Cebpa的启动子H3K27三甲基化来抑制Cebpa的转录,从而抑制BMSCs向脂肪细胞分化。因此,Bmi-1可以通过表观遗传调控BMSCs分化来延缓骨衰老。
该论文主要由基础医学院人体解剖学系硕士研究生赵景钰、陈傲和教师王嵘等完成,靳建亮教授和我校附属口腔医院王羽立副教授为本文通讯作者。该研究主要在国家自然科学基金面上项目和江苏省青蓝工程基金项目的资助下完成,并得到了苗登顺教授和张永杰教授的指导与帮助。
原文链接:http://doi.org/10.1002/advs.202404518
(供稿/靳建亮课题组;审核/陈峰 王觉进)

