为强化科技伦理风险防控,促进负责任创新,依据《中华人民共和国科学技术进步法》《关于加强科技伦理治理的意见》《科技伦理审查办法(试行)》(国科发监〔2023〕167号)等法律法规和相关规定,涉及人的生命科学和医学研究的项目,需申请伦理审查。
根据我校实际工作需要,科技项目伦理申请分“项目申报预审查”和“常规伦理审查”两类。
一、伦理审查系统登录方式
登录南京医科大学融合门户https://i.njmu.edu.cn,搜索“科技伦理审查系统”,仔细阅读界面弹出的“申请人须知”后,进入服务。
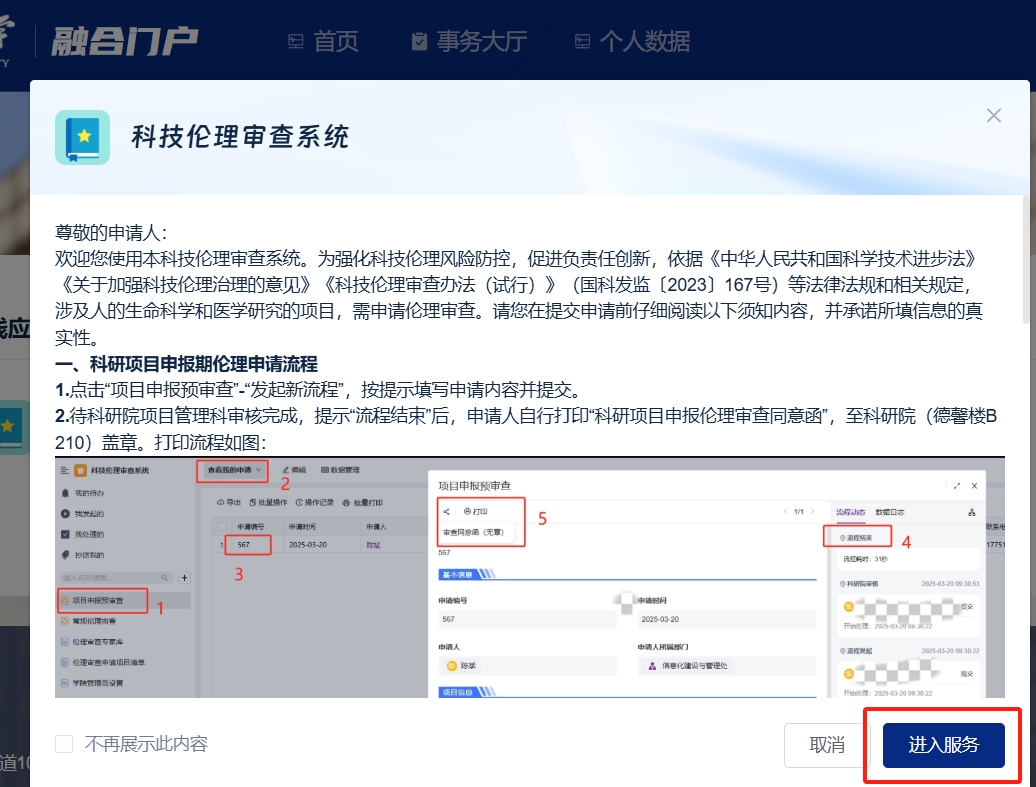
注:①登录账户需为学校教职工,学生无权限申请;
②原则上由项目负责人发起伦理申请。
二、科研项目申报期伦理申请流程(适用于项目申报期)
1.申请人登录“科技伦理审查系统”后,点击“项目申报预审查”-“发起新流程”,按提示填写申请内容并提交科研院待审核。
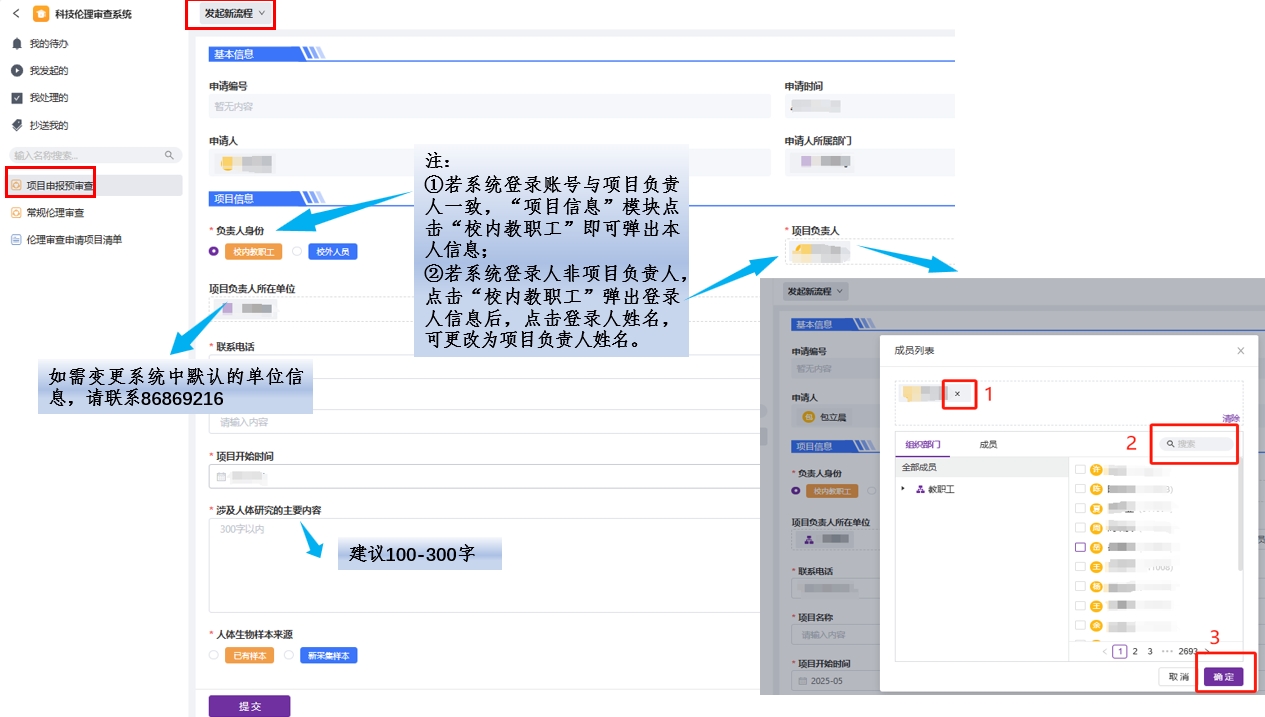
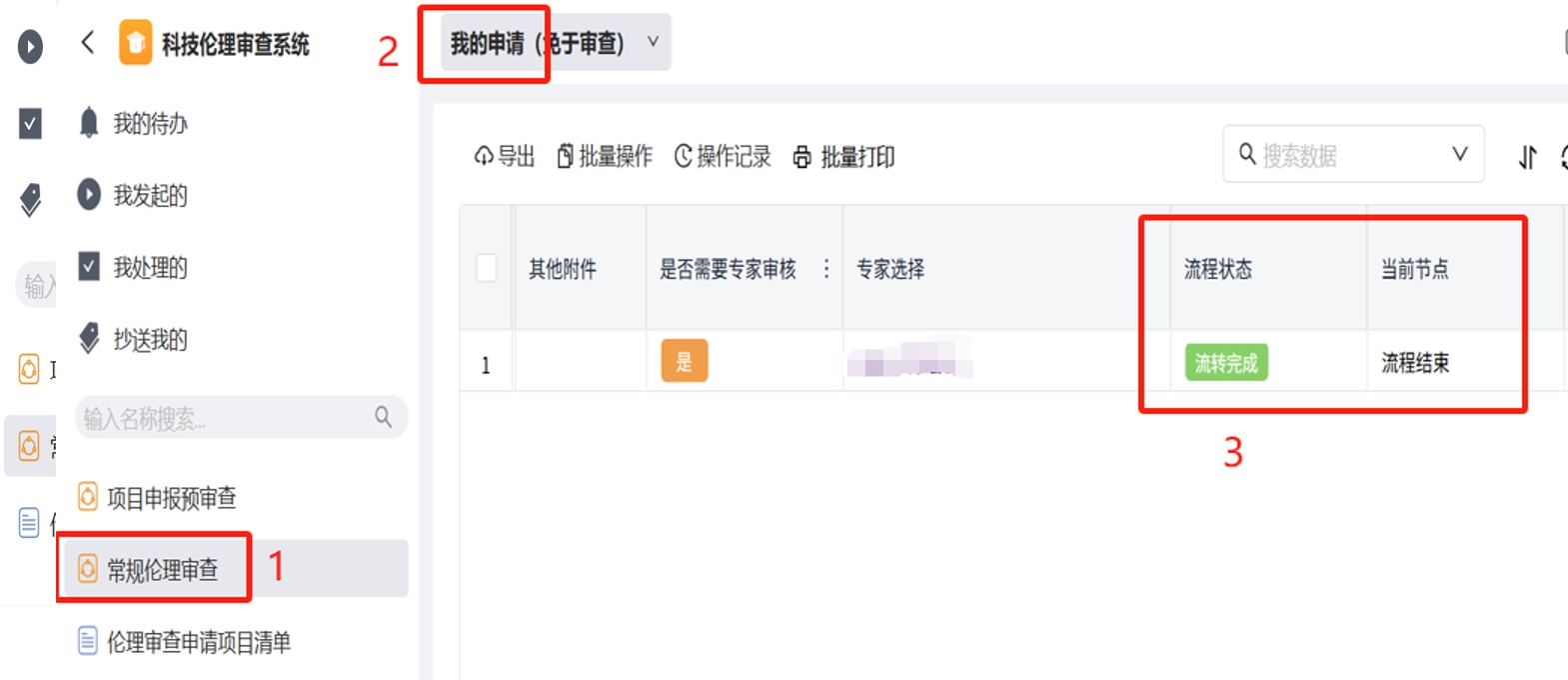
2.申请人可点击“项目申报预审查”-“查看我的申请”查看审核状态。待页面提示“流转完成”,即科研院审核完成。
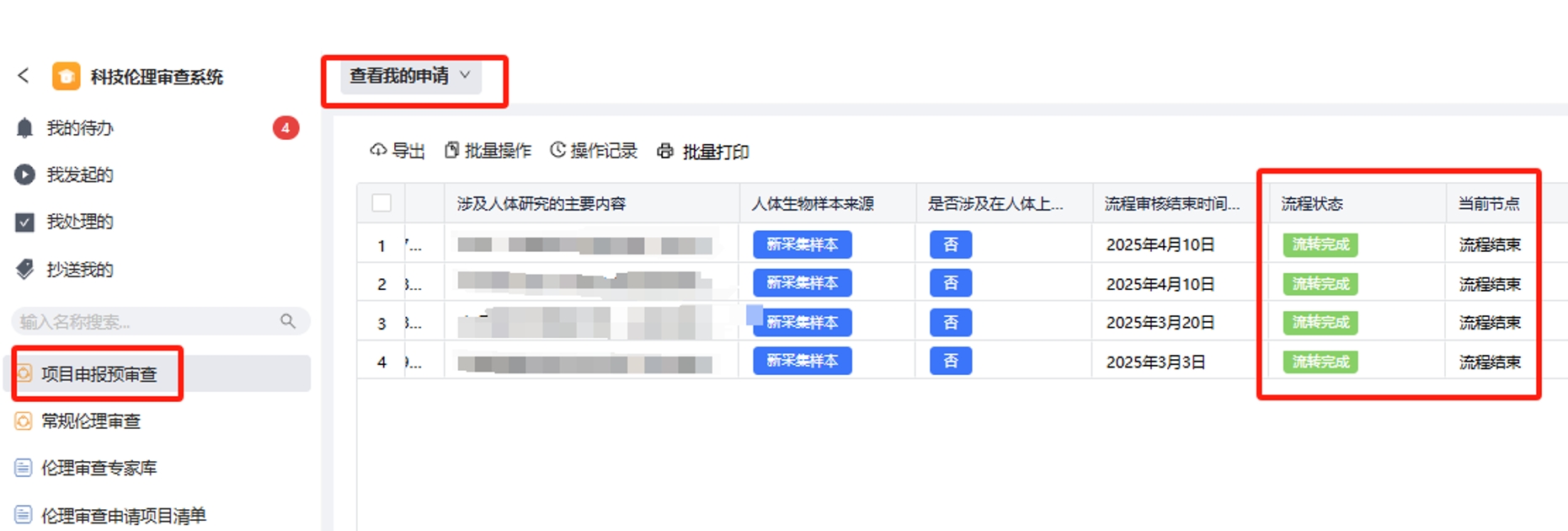
请申请人自行打印“科研项目申报伦理审查同意函”,至科研院(德馨楼B210)盖章。打印流程如图:
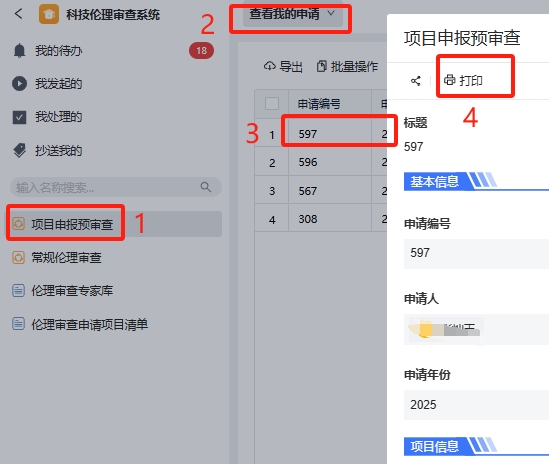
注:科研项目申报伦理批件仅供项目申报使用。项目获得立项批准,该批件即宣告失效,并需依据相关规定重新进行正式伦理审查申请。
三、常规伦理审查申请办理流程(主要适用于项目获立项批准后)
1.申请人登录“科技伦理审查系统”后,点击“进入服务”- “常规伦理审查”-“发起新流程”-“选择数据”。
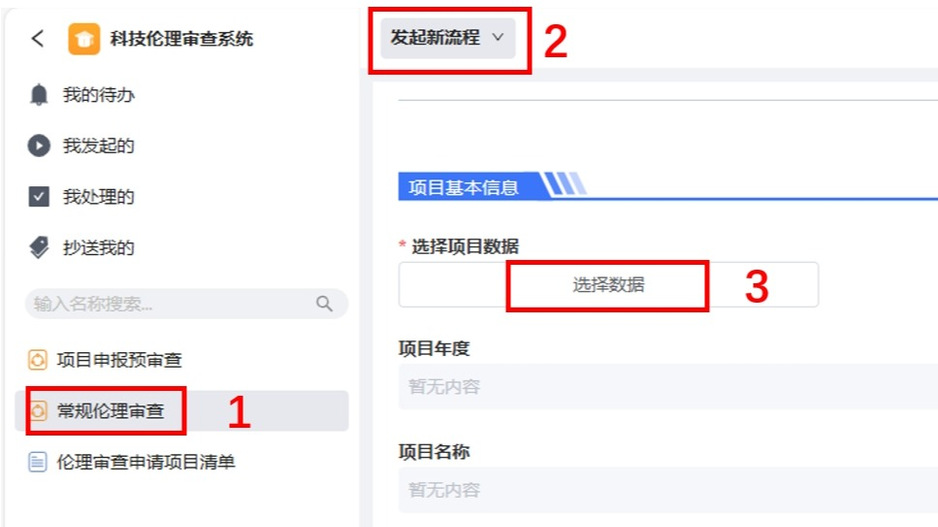
2.申请人按照以下要求填写“选择数据”板块。
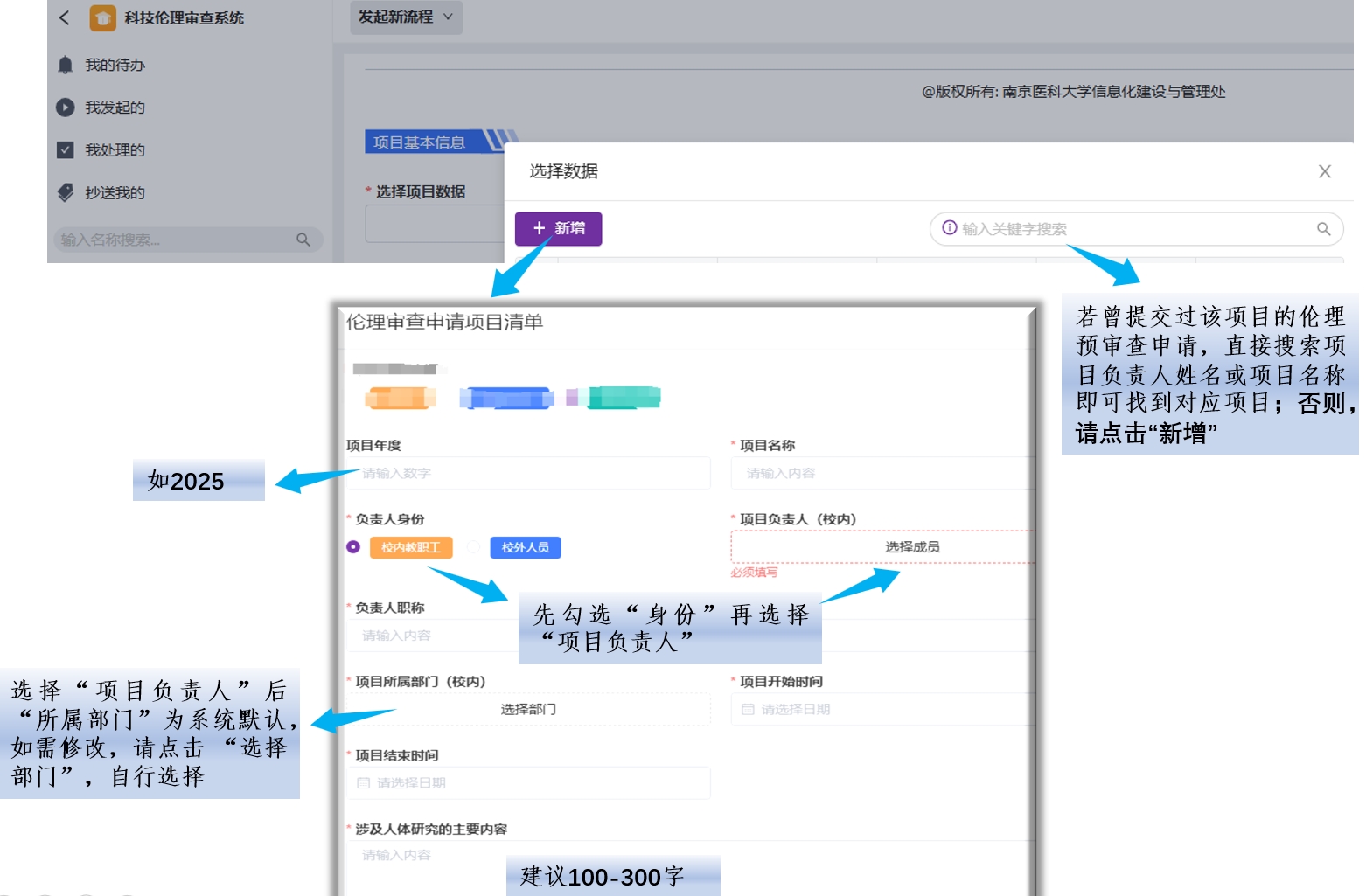
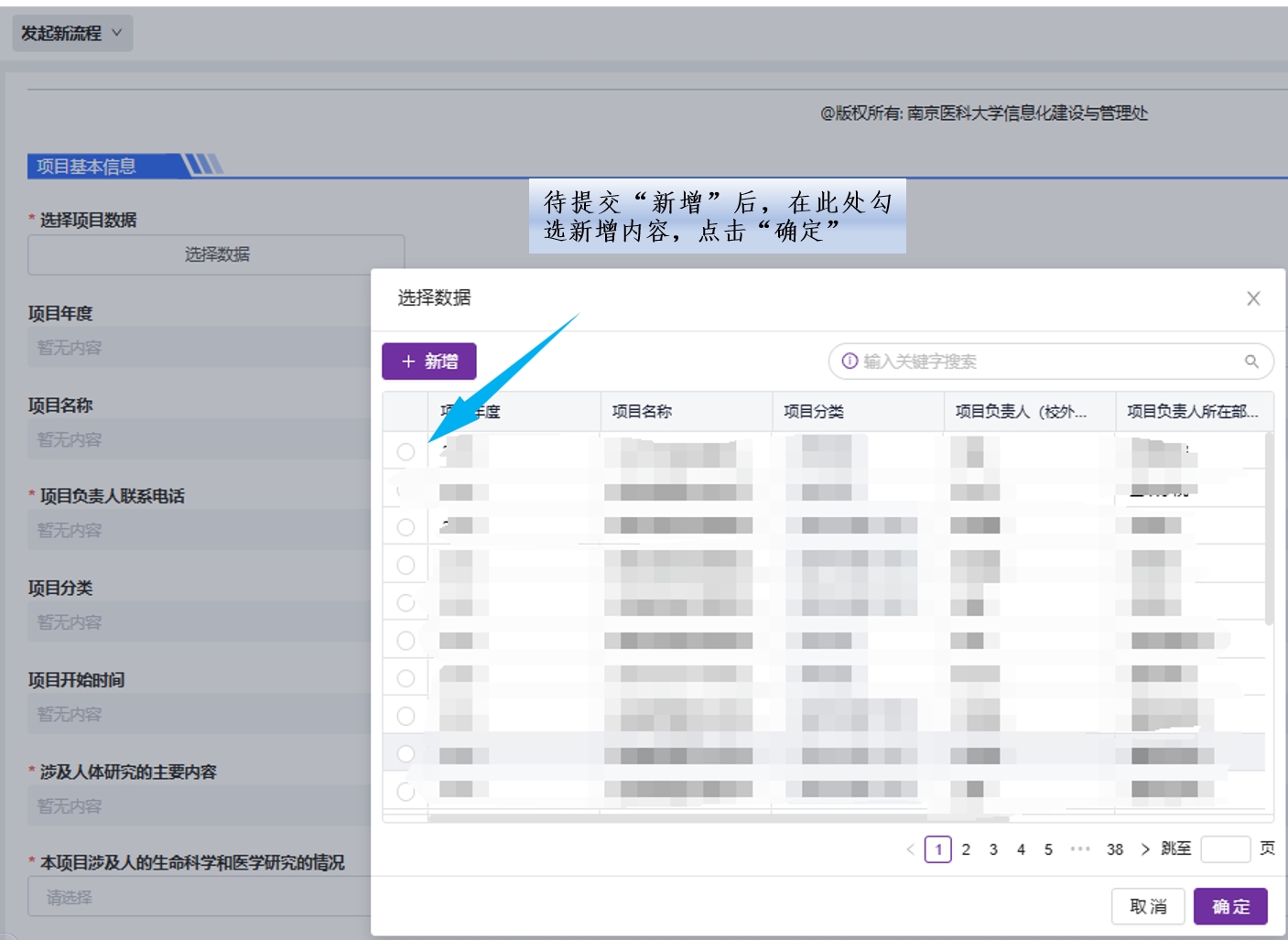
3.关于“本项目涉及人的生命科学和医学研究的情况”的填写说明:
l 适用情况
①利用合法获得的公开数据、匿名化的信息数据,或者通过观察且不干扰公共行为产生的数据进行研究的;
②使用已有的人的生物样本开展研究,所使用的生物样本前期已通过伦理审查,研究相关内容和目的在规范的知情同意范围内的;
③使用人源细胞株或者细胞系等开展研究,研究相关内容和目的在提供方授权范围内的;
④采用调查、访谈方法的研究;记录声音、视频、数字或者影像的数据采集;
⑤利用常规健康体检、临床常规非侵入性检查或已经批准应用的医疗器械检测人体指标的研究;
⑥需新采集人体细胞组织血液等样本来开展的研究;
⑦采用新技术或者新产品在人体上进行的试验研究。
l 若本项目“涉及人的生命科学和医学研究的情况”仅属于①-③范畴,“请求审查类型”请选择“免于审查”并提交免于审查申请表(手写签名后上传pdf版本)及项目申请书;
l 若本项目“涉及人的生命科学和医学研究”存在属于情况④-⑤的,“请求审查类型”请选择“简易审查”并提交研究方案及知情同意;
l 涉及情况⑥,在医疗机构采集人体组织血液样本的,应先取得相应单位的伦理许可;
l 涉及情况⑦的,请联系临床研究伦理委员会,86869732。
4.审核:
•申请人提交后,申请将被自动推送所在院系的院长/主任进行审核。
•学院审核通过后,由科研院依据研究内容安排伦理专家开展审查,审查周期约2周。若任何一位专家审核不通过,申请人需根据退回意见修改后再次提交复审。
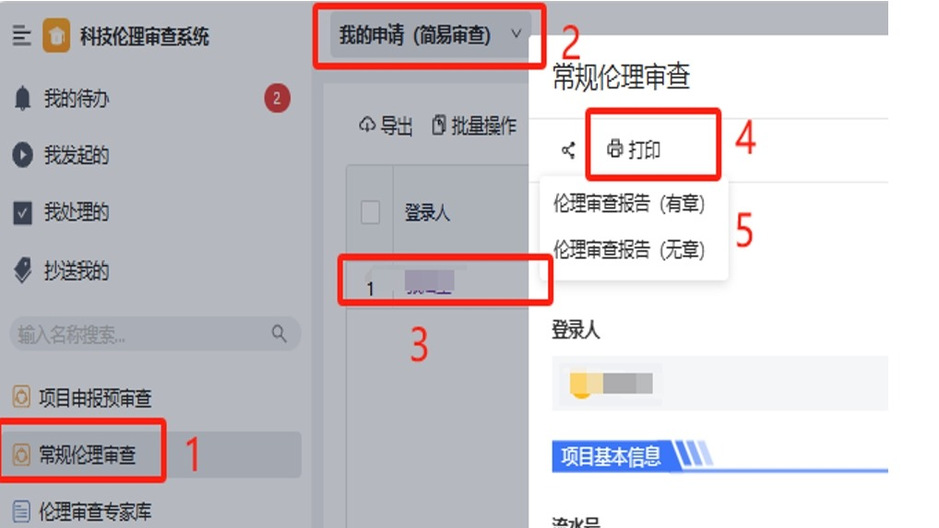
•申请人可点击“常规伦理审查”-“我的申请”查看审核状态。待提示“流转完成”,即可下载伦理报告。
•如需盖章原件,请申请人自行打印“伦理审查报告(无章)” 版本,至科研院(德馨楼B210)加盖印章。打印流程如图:
注:如需英文批件,须在申请流程结束后,对照中文版自行编制英文版报告,并将中英文报告纸质版本同时递交至科研院予以用印。
四、跟踪审查
常规纵向项目将年度报告作为跟踪审查的材料和依据,如果涉及人的研究方案有重大变动的,应主动提交变更方案。
五、审查周期
•学期中:1个月内;寒暑假期:2个月内
•具体时间与频次将根据项目申请实际情况酌情调整,请留意相关通知。
六、申请时间要求
•伦理审核通过后方可开展项目研究,原则上不接受事后补充伦理审查申请。
七、联系方式与办公地址
•办公地址:江宁校区德馨楼B210办公室
•联系人:张灿玉
•联系电话:86869216
•盖章时间:工作日16:00-16:30,否则不予处理。

